有机质谱分析解析
有机质谱
质谱,即质量的谱图,物质的分子在高真空下,经物理作用或化学反应等途径形成带电粒子, 某些带电粒子可进一步断裂。
每一离子的质量与所带电荷的比称为质荷比(m/z,曾用 m/e)。不同质荷比的离子经质量分离器一一分离后,由检测器测定每一离子的质荷比及相对强度,由此得出的谱图称为质谱。
分子被电子束轰击失去一个电子形成的离子称为分子离子。分子离子用 M+·表示。分子离子是一个游离基离子。在质谱图中与分子离子相对应的峰为分子离子峰。分子离子峰的质荷比就是化合物的相对分子质量, 所以,用质谱法可测分子量。
含有同位素的离子称为同位素离子。在质谱图上, 与同位素离子相对应的峰称为同位素离子峰。
分子离子在电离室中进一步发生键断裂生 成的离子称为碎片离子。
经重排裂解产生的离子称为重排离子。其结构并非原来分子的结构单元。在重排反应中, 化学键的断裂和生成同时发生, 并丢失中性分子或碎片。
具有未配对电子的离子为奇电子离子。这样的离子同时也是自由基,具有较高的反应活性。无未配对电子的离子为偶电子离子。
分子中带有不止一个电荷的离子称为多电荷离子。当离子带有多电荷离子时, 其质核比下降, 因此可以利用常规的四极质量分析器来检测大分子量化合物。
从离子源出口到检测器之间产生的离子。即在飞行过程中发生裂解的母离子。由于母离子中途已经裂解生成某种离子和中性碎片, 记录器中只能记录这种离子, 也称这种离子为亚稳离子, 由它形成的质谱峰为亚稳峰。
比分子量多或少 1 质量单位的离子称为准分子离子,如:(M+H)+, (M-H)+。其不含未配对电子, 结构上比较稳定。
分子离子是质谱图中最有价值的信息,它不但是测定化合物分子量的依据,而且可以推测化合物的分子式, 用高分辨质谱可以直接测定化合物的分子式。
一般来讲, 从分子中失去的电子应该是分子中束缚最弱的电子, 如双键或叁键的π电子, 杂原子上的非 键电子。
分子离子的丰度主要取决于其稳定性和分子电离所需要的能量。易失去电子的化合物,如环状化合物,双键化合物等,其分子离子稳定,分子离子峰较强;而长碳链烷烃,支链烷烃等正与此相反。
各类化合物分子离子稳定性次序大致为:芳香环 (包括芳香杂环) >共轭烯> 烯 > 脂环 > 硫醚,硫酮> 酰胺 > 酮 > 醛 > 直链烷烃> 醚 > 酯 > 胺 > 羧酸>腈>伯醇>仲醇>叔醇>高度支链烃。
芳环 (包括芳杂环) 、 脂环化合物、 硫醚、 硫酮、 共轭烯分子离子峰比较明显,直链酮、 酯、 酸、 醛、 酰胺、 卤化物等通常显示分子离子峰,脂肪族醇、胺、 亚硝酸酯、 硝酸酯、 硝基化合物、 腈类及多支链化合物容易裂解, 分子离子峰通常很弱或不出现。
分子离子峰不出现或丰度极低难以确认, 可根据不同情况改变实验条件予以验证。
将常用的70eV 改变15eV 以减少形成的分 子离子继续断裂的几率, 降低了碎片离子的丰度, 使分子离子峰的相对丰度增加, 从而可能辨认出分子离子。
降低轰击电子能量的结果会使仪器的灵敏度 下降, 虽然分子离 子峰的丰度有所提高, 但离子的绝对强度降低,一些由于热不稳定和低挥发性等原因而不出现分子离子峰的化合物, 用这种办法不会得到预期的效果, 这时可采取各种软电离的办法, 虽然碎片离子大量减少, 但可以突出分子离子峰。
气化温度的降低可以减少分子离子进一步断裂的可能性, 分子离子峰的相对丰度增加。如三十烷烃在340℃时气化, 不出现分子离子峰,改变70℃气化时分子离子峰的丰度接近基峰。
某些化合物不易挥发或热稳定性差,可以衍生化处理。例如, 可将某有机酸制备成相应的酯, 酯容易气化, 而且易得到分子离子峰, 由此来推断有机酸的分子量。
解析时一般把谱图中最高质荷比的离子假设为分子离子,后用分子离子的判别标准一一
对比,若被检查离子不符其中任何一条标准,则它一定不是分子离子;若被检查离子符合所有条件, 则它有可能是分子离子。分子离子的判别可以参考如下标准:
(1)分子离子必须是奇电子离子。由于有机分子都是偶电子,所有失去一个电子生成的分子离子必是奇电子离子。
(2)是否符合氮规则 (Nitrogen Rule) 。有机化合物的分子量是偶数或奇数与所含有的氮原子的数目有关。凡不含氮原子或含偶数个氮原子的化合物, 其分子量必为偶数;含奇数个氮原子的化合物, 其分子量必为奇数, 这就是所谓的氮规则。
(3)合理的中性碎片的丢失。这些中性碎片可能是小分子或者自由基基团。这些中性碎片有着特殊的质量数, m/z最高值与邻近的碎片离子之间应有一个合理的质量差。
例如: M+丢失一个质子H, CH3, H2O,C2H4等是合理的。如果这个质量差落在4~14和21~25之间就是不合理的, 也即如果在M-4到M-13的范围内存在峰, 则说明原所假定的分子离子峰不是分子离子峰。
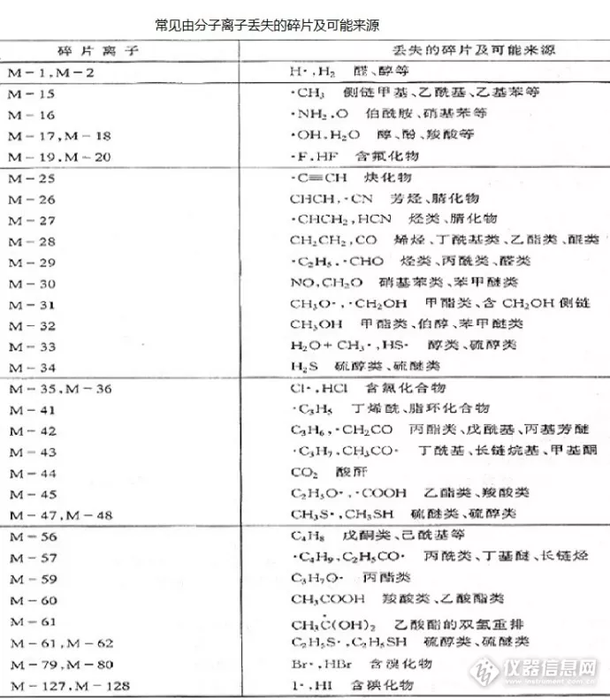
碎片离子的质荷比及其丰度在质谱数据中占很大比例。碎片离子的相对丰度与分子结构有密切关系,高丰度的碎片峰代表分子中易于裂解的部分,如果有几个主要碎片峰,并且代表着分子的不同部分, 则由这些碎片峰就可以粗略地把分子骨架拼凑起来。质谱解析的大量工作就是分析碎片离子的形成过程。
分子失去电子,形成游离基离子,它的电子有强烈的成对倾向,电子转移与邻近原子形成一个新键,同时邻近原子的α键断裂。因此,这种断裂通常称为“α”断裂反应。
(1)饱和杂原子:杂原子的孤对电子电离能较低,很容易去失,形成游离基离子,进而发生α断裂,如
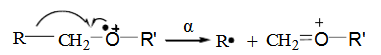
(2)不饱和杂原子:例如羰基化合物的α断裂过程如下
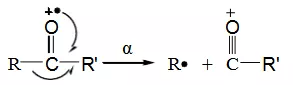
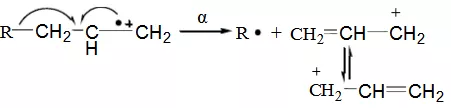
上述反应的进行与游离基中心给电子倾向有密切的关系。氮原子给电子能力很强,α断裂在脂肪族胺中占主导地位,其次是氧族元素,由给电子能力的差别造成的α断裂反应的难易程度按下列顺序排列:N>S、O、π,R﹒>Cl、Br>H。当一个化合物有几个α键时,最容易去失的是最大的烷基游离基。
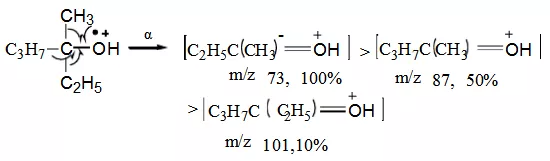
2、i断裂(诱导断裂)诱导断裂是由正电荷诱导、 吸引一对电子而发生的断裂, 其结果是正电荷的转移。诱导断裂常用i来表示。一般情况下, 电负性强的元素诱导力也强。在有些情况下, 诱导断裂和α断裂同时存在,。由于i断裂需要电荷转移, 因此,i断裂不如α断裂容易进行。表现在质谱中, 相应α断裂的离子峰强,i断裂产生的离子峰较弱。例如乙醚,i断裂和α断裂同时存在, α断裂的几率大于i断裂。但由于α断裂生成的m/z 59还有进一步的断裂,因此在乙醚的质谱中, m/z59并不比m/z 29强。
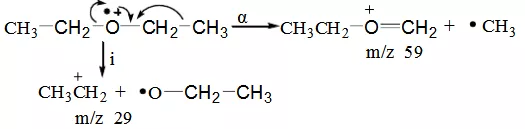
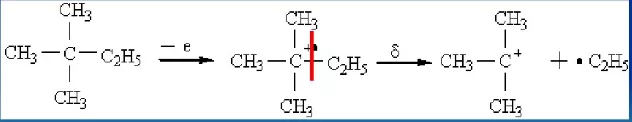
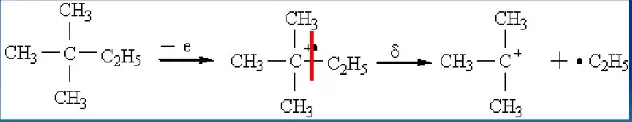
3、σ断裂如果化合物分子中具有σ键, 如烃类化合物, 则会发生σ键断裂。σ键断裂需要的能量大, 当化合物中没有π电子和n电子时, σ键的断裂才可能成为主要的断裂方式。断裂后形成的产物越稳定, 这样的断裂就越容易进行,阳碳离子的稳定性顺序为叔>仲>伯。因此, 碳氢化合物最容易在分支处发生键的断裂。并且, 失去最大烷基的断裂最容易进行。
重排开裂时涉及到两个键的断裂,脱去一个中性分子,同时发生H重排。重排的结果产生了在原化合物中不存在的结构单元的离子。
(1)麦氏重排(Mclafferty rearrangement)
分子离子或碎片离子结构中有 双键, 且在γ位上有H原子的正离子都能发生麦氏重排。在开裂中, γ位上的H通过六元环过渡态的迁移到电离的双键碳或杂原子上, 同时烯丙键断裂, 生成中性分子和碎片离子。
醛、 酮、 羧酸、 酯、 酰胺、 碳酸酯、 磷酸酯、 肟、腙、 烯、炔以及烷基苯等的含有γ-H的有机化合物很容易发生麦氏重排。
(2)逆迪尔斯一阿尔德重排(retro Diels-Alder fragmentation,RDA)
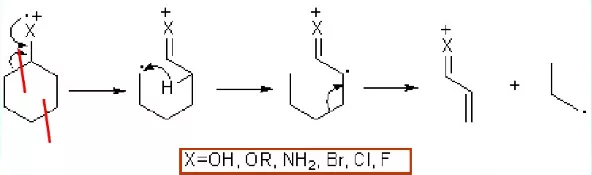
对具有环内双键结构的化合物能发生RDA开裂, 一般生成一个带正电荷的共轭二烯自由基和一个中性分子。
在一些醇类、 硫醇类、 卤代烃等有机化合物分子的质谱中经常出现脱去水、硫化氢、 卤化氢等小分子化合物而生成的碎片离子。醇非常容易脱去水分子, 所以醇类化合物的分子离子峰相对丰度很小, 甚至不出现分子离子峰。
复杂开裂是指在有机化合物的质谱中,经常出现离子中两个或两个以上化学键连续发生断裂生成碎片的过程。·除了重排反应以外, 环状化合物的质谱碎裂也是如此。复杂断裂一般是指环状化合物发生的多个键断裂, 有时涉及一个氢原子的转移。
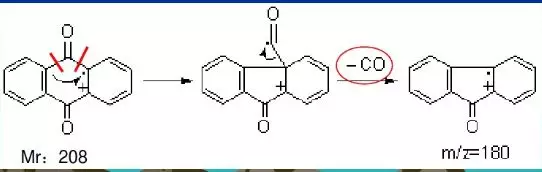
骨架重排是指在有机化合物裂解过程中, 部分基团如甲基、 芳香基以及含O、N、S等的基团发生迁移,生成一些小的中性碎片、自由基离子等的过程。常见的中性碎片如CO、SO、SO2, S2, CH=CH等。如蒽醌发生芳基迁移, 存在下列裂解:

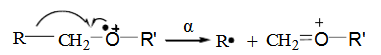

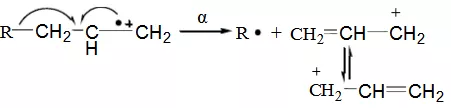
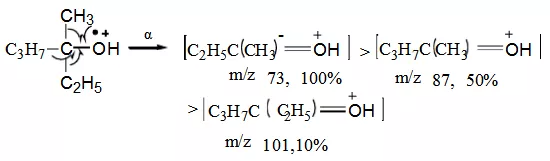
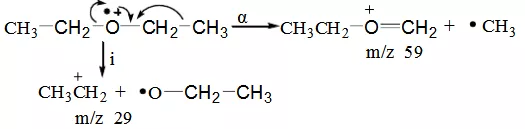













加载更多