四种滴定分析法大比拼,你pick哪个?
1.酸碱滴定法:
它是以酸、碱之间质子传递反应为基础的一种滴定分析法。可用于测定酸、碱和两性物质。其基本反应为:H++OH-=H2O
2.配位滴定法(络合滴定分析):
它是以配位反应为基础的一种滴定分析法。可用于对金属离子进行测定。
3.氧化还原滴定法
它是以氧化还原反应为基础的一种滴定分析法。可用于对具有氧化还原性质的物质或某些不具有氧化还原性质的物质进行测定,如重铬酸钾法测定铁,其反应如下:
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
4.沉淀滴定法
它是以沉淀生成反应为基础的一种滴定分析法。可用于对Ag+、CN-、SCN-及类卤素等离子进行测定,如银量法,其反应如下:Ag++Cl-=AgCl
(一)共同点:
1.他们都是以消耗计算量的标准物质来测定被测物质含量的。
2.随着滴定剂的加入,被滴定物质的浓度在计量点附近会有突变(突跃),可以用这一突变,或通过这一突变导致指示剂的变色来制定滴定终点。
3.滴定分析终点误差的定义都可以表示为Et={【(cV)T-(cV)X】/(cV)X}*100%。
4.由于历史遗留问题四者使用的常数不同,若都用滴定常数Kt,可使四种滴定数学处理趋于一致。
(二)不同点:
1.强酸强碱的滴定产物为水,从滴定未开始到滴定结束H2O一直是一个常数,约为55.5mol/L。
2.沉淀滴定有异相生成随着滴定的进行,一旦有沉淀生成他的活度就被制定为1,并且保持不变。
3.络合滴定产物ML的浓度在滴定过程中是一变量开始时为0,随着滴定的进行,ML的浓度近线性的增大,直至化学计量点。
4.最简单的氧化还原反映的滴定产物有两种,他们在滴定过程中的浓度变化与络合滴定产物ML相似。所以从这一意义上,可把滴定分析分为两种,一种是滴定产物的浓度为常量的,如强酸强碱滴定、沉淀滴定;一种是产物为变量的,如络合和氧化还原滴定。
指示剂在分析滴定中是一支神奇的“魔棒”他指示着我们实验的进程,以便使我们知道什么时候开始以及什么时候结束。
酸碱指示剂:一些有机弱酸或弱碱,它们的酸式或碱式具有不同的颜色。
金属指示剂:与酸碱指示剂不同,它不是以指示溶液中H+的浓度变化确定终点,而是以指示溶液中金属离子的浓度变化确定终点。
氧化还原指示剂:一些有机物随氧化还原电位变化而改变颜色,从而达到指示终点的目的。
吸附指示剂:它是沉淀指示剂中的一类特殊指示剂。
(1)酸碱指示剂
以酚红为例:
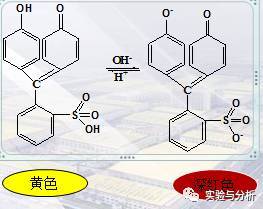
(2)金属指示剂
M +In=MIn
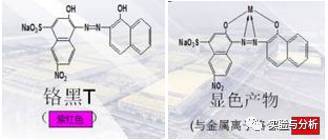
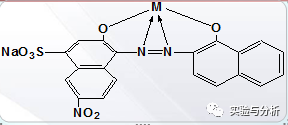
铬黑T是个二元弱酸,以H2In-表示。随着溶液的pH值的升高,它分两步电离,且在溶液中呈现出三种不同的颜色:
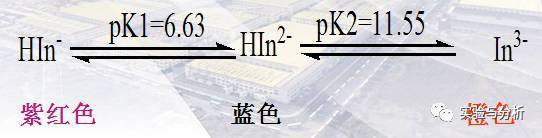
(3)氧化还原滴定指示剂
二苯胺磺酸钠为例:

(4)沉淀指示剂
吸附指示剂的原理是有机物离子被沉淀吸附,这种吸附与沉淀表面的电荷密度有密切关系。一旦被吸附,通过沉淀上的电荷与指示剂的电子系统互相作用,指示剂被极化,引起电子能级的变动,使指示剂的吸收光谱发生或大或小的变化,分散在溶液中的沉淀颗粒优先吸附它们自己的离子,已经证实,大多数吸附指示剂纯粹依赖于共沉淀后的极化作用。
指示剂的适用条件:
1.每种酸碱指示剂都有一定的变色范围。
2.金属指示剂络合物与指示剂的颜色有明显区别,终点颜色变化才明显。金属指示剂络合物稳定性应比金属EDTA络合物的稳定性要低。
3.氧化还原指示剂是一种通用的指示剂,应用比较广泛。
4.尽量使沉淀表面积大些。
各指示剂的缺点与不足:
1.酸碱指示剂的变色间隔是人的目视确定的,不同的人对颜色敏感度不同,因而观察的变色间隔也不同。
2.金属指示剂在使用中也存在弊端:指示剂有封闭现象、僵化现象同时指示剂也会氧化变质。
3.在不可逆氧化还原指示剂的使用中也存在缺陷:因为它们可被过量的滴定剂氧化产生有色或无色产物,虽然加入过量的还原剂但此过程不会反过来,而且由于氧化剂局部浓度过高,可能导致颜色变化过早从而得到在化学计量点之前指示终点的错误。再者对于被指示剂消耗的滴定剂量,一定要使用校正值。
4.吸附指示剂由于受其吸附能力的大小限制,使其应用范围大为缩小。
小结
在四大平衡的滴定中,我们经常要使用各种指示剂。只有对指示剂有足够的了解,才能在实际操作过程中对指示剂做出正确的选择与应用。运用过程中,要注意指示剂的适用pH范围、温度、离子强度以及指示剂是否变质等条件。要想使实验的结果正确,必须以科学严谨的态度注重每个细节。
展源
何发
相关文章
-

电位滴定法进行酸碱滴定
2020-05-27
-

电位滴定法可以进行酸碱滴定
2020-05-27
-

多元校正滴定法测定酒石酸美托洛尔
2020-05-27
-

干货丨电位滴定法确定滴定终点方法介绍
2021-08-27
-

电位滴定法中确定滴定终点的4种方法
2020-05-27
-

用多元校正滴定法测定酒石酸美托洛尔
2020-05-27
-

原料药含量测定:HPLC法or滴定法?
2020-05-27
-

电位滴定法及其在药物分析中的应用
2021-12-06
-

氧化还原滴定曲线及其滴定终点的确定
2020-05-27
-

酸碱滴定or电位滴定,石油酸值检测你选哪种?
2022-06-30

加载更多