IDMS法测定血清中的生长激素
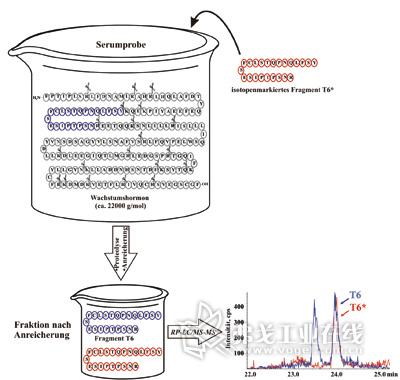
图1. 生长激素的IDMS测定法示意图:将“指纹碎片”T6以胰蛋白酶进行蛋白质水解,并对分析溶质予以富集后,借助于RP-LC-MS/MS进行定量测定。
在医学上,为了进行早期诊断以及对疾病进行医疗控制,经常需要对血清中的所谓标记蛋白质进行量化。这些蛋白质分子尺寸微小,结构复杂,血清蛋白浓度需在超过10个数量级的动态范围中进行定量测定,为准确的分析方法建立提出了挑战。
人类的生长激素由脑垂体产生,这是一种由多种蛋白变异体(亚型)构成的异质性产物。除了22 kDa(千道尔顿)分子量的主要组分外,还具有20 kDa分子量的亚型以及更小的变异体。由于生长激素的供应不足会导致儿童侏儒症,而供应过度又会造成成年人肢端肥大症或儿童巨人症,生长激素的测定被用于对疾病进行诊断。在生长激素定量测定的例行分析方法中,免疫测试法并未将亚型加以区分,这样做虽然灵敏度较高,然而可能存在因试剂盒不同而导致结果偏差较大的缺点。产生这种偏差的原因在于,采用的垂体萃取物是含有亚型混合物,因试剂盒的具体情况而异;另外,试剂盒所用的具有选择性的抗体所引起的交互反应也是一个原因。
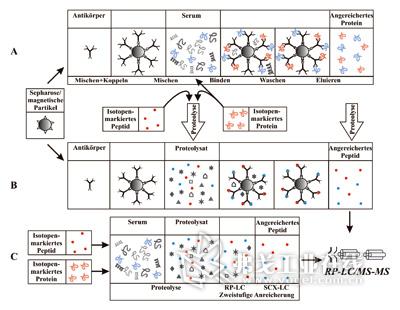
图2. 将分析溶质从样品基体中进行分离富集,然后用LC-MS/MS进行定量测定的示意图。
同位素稀释质谱法IDMS
同位素稀释质谱法(IDMS)相比免疫法而言受到基体的影响较少。对于血清中低分子量的诊断标记物的定量测定,如甾体激素,已建立了成熟的方法。鉴于最常用的血清白蛋白和靶蛋白质如人类生长激素之间的浓度差别高达7个数量级,因此采用IDMS法必须预先进行基体分离并富集分析溶质,减少抑制离子化而引起的信号降低以及所伴随的灵敏度损失。为了用IDMS法进行标记蛋白质定量,拟采用蛋白质组学的样品前处理方法,针对靶蛋白质有代表性的“指纹碎片”,蛋白质水解后借助于胰蛋白酶或者其它的蛋白酶进行测定(见图1)。图1是对掺入垂体萃取物的血清样品进行定量的离子谱图(测得浓度为12 μg/L),为T6以及T6*专用的MS-MS过渡所摄制。碎片T6和内标T6*分别以蓝色(T6)和红色(T6*)显示,在生长激素序列中,胰蛋白酶的碎片化通过剪刀进行标记,而氨基酸的序列按照字母顺序表示。

图3. 人类22 kDa生长激素的氨基酸序列图。胰蛋白酶分裂为赖氨酸(K)和精氨酸(R),这些氨基酸以深灰色表示,用于定量测定的碎片位于灰色之中。
富集方法
靶蛋白质可以直接在血清中进行富集,此时必须采用以同位素标记过的完整蛋白质作为内标,旨在对富集过程中靶蛋白质的损失进行补偿。靶蛋白质可通过免疫沉淀法借助于固定的抗体进行富集(见图2A)。为了进行定量测定,可采用多克隆的抗体,这样对靶蛋白质亚型一并富集的概率更大。将所富集的萃取物进行蛋白质水解反应,选择碎片作为完整蛋白质的代表,以IDMS法进行测定。这种富集方法的缺点在于以同位素标记的完整蛋白质只有较小的可用性。
另一种方法是首先将全部血清进行蛋白水解,将所选取的靶分子碎片与干扰性的基体部分进行分离,最后以IDMS法进行测定。当碎片被完全水解,定量地从靶蛋白中释放出来的前提条件得到满足时,可将同位素标记的碎片作为内标,通过此富集方法进行应用。这种方法容易通过化学合成实现,同时也较为廉价。分析溶质从蛋白质中释放地越缓慢,则相对内标出现的结构差别就越大,通过同位素标记的碎片进行补偿就更难完全。需注意的是,所选用的碎片必须是化学上稳定的,而环境条件应使水解反应快速进行,以便获得蛋白定量的高度准确性。当采用以同位素标记的完整蛋白质为内标时,就避免了由于不完全水解所产生的问题,碎片的释放仿照靶蛋白进行。
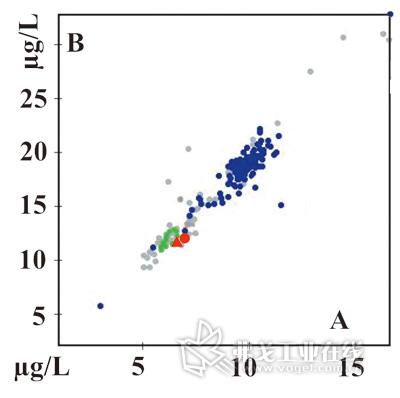
图4. 两种控制材料HP1/08A和B中生长激素的测定:蓝色属于西门子医药系统,绿色属于意大利Diasorin公司,灰色为其它制造商提供,红色圆圈为基于T6的IDMS测定结果,红色三角为基于T12的IDMS测定结果。
碎片及其同位素标记的对应物的富集可以如同处理完整蛋白质一样,通过免疫沉淀法固定于一种对碎片具专属性的抗体上(见图2B)。如果采用单一型抗体代替多重型克隆型抗体,则富集的选择性会有所提高。一种变通的富集方法是采用半制备式液相色谱法(见图2C),分步地采用半制备反相液相色谱以及强酸性阳离子(SCX)交换色谱。以结扣所示的靶蛋白质以及它的以圆圈表示的碎片均通过颜色加以凸显(见图2C):天然的为蓝色,同位素标记的为红色,其它的血清和蛋白水解物的基体成分则以灰色表示。相对于免疫富集法必须针对每种所选的碎片配置以专门的抗体而言,这种液相色谱法的优点在于具有较高的灵活性,选择能够代表靶蛋白质的碎片进行IDMS法测定。
实验过程
人们按照需定量测定的靶蛋白质所相应的亚型来选择稳定性良好的碎片,碎片的质谱检测法需要具有足够的灵敏度,借助于数据库选择碎片时,可避免与其它血清蛋白质序列的重叠。
人类生长激素的质谱测定法,是对总血清加入胰蛋白酶来进行前述的蛋白质水解,继以液相色谱法对两种碎片T6和T12(见图3B)及其同位素标记的对应物进行分离,所测结果的浓度范围为3~30μg/L。
将两种碎片T6和T12通过二维半制备液相色谱进行提纯。第一步是于反相柱(RP柱)上进行预分离。截取富集的T6 和 T12馏分,然后以强酸性阳离子(SCX)交换色谱法进行进一步提纯。在采用C18小管以固相萃取法除掉盐分后,就可将所富集的碎片通过由反相色谱法联合串联质谱检测器进行定量测定(LC-MS/MS)。根据蛋白质水解反应后从生长激素中释放出来的碎片信号,与水解前加入到血清中的同位素标记的标准所产生的碎片信号之间的比例关系,就能够测出样品中生长激素的含量。为了加入确定的生长激素和标准,采用了高纯的储备溶液,储备溶液的浓度通过将参照物质分裂为氨基酸后以IDMS法进行氨基酸分析。
为了验证IDMS法对生长激素的测定,将准确含量的重组22 kDa生长激素和同位素标记的标准物加入到一种血清样品中,该样品是不能采用前述方法进行验证的。将这种含添加物的血清样品中所测得的浓度与通过加入生长激素而调制成的数值进行比较,就能够验证定量方法的准确性。数次测量值的中位值相对于期望值的偏差,对于两种碎片T6和T12而言,均小于结果的相对标准偏差。所测得的浓度表明与期望值之间没有显著的偏差。
与免疫分析法的比较
传统的商用检测手段所进行的质量控制结果,其分散性超过了临床上重要的生长激素的浓度范围。而采用IDMS法对生长激素进行的测定,虽然对于例行诊断而言时间会相对紧张,但却能够为控制材料提供准确的参考数值。对这两类参考材料中的生长激素进行了补充性量化测定,对照174个检测实验室的结果,所测结果见图4。
检测限的降低
在实验室医学诊断中,对肢端肥大症进行抑制试验。血清中生长激素的浓度应该由抑制制葡萄糖的剂量而降低到1 μg/L以下,以排除肢端肥大症。为了在将来也能够采用IDMS法来定量测定抑制试验中生长激素的浓度,必须提高测定方法的灵敏度,目前按照线性相关法从校正曲线计算出的检测限对于T6 和 T12分别为1.7和2.7 μg/L。这种IDMS法还不够灵敏,不足以将激素的生理体液抑制到低于1μg/L时进行显示。当前正在研究是否能够通过改善分析富集的方式来降低检测限。
作者简介

Christian Arsene博士:1991~1997就读于汉堡大学化学专业,1998~2002于布伦瑞克大学取得博士学位,博士论文“鳞翅类中长链脂肪的结构解析与反应研究”,2003~2005任职于瑞士Buchs西格玛奥德里奇公司化学发展部,2005起任职于布伦瑞克联邦物理技术局(PTB)生物有机分析组。
德国联邦物理技术研究院(PTB)生物有机分析组
展源
何发
热点文章
-
【必看】实验滴定终点变色顺口溜
2026-03-24
-
提效增能·创新提质 色谱质谱助力食品安全技术能力建设
2026-03-24
-
HJ 166-2026 土壤环境监测技术规范
2026-03-03
-
液质联用仪(LC-MS/MS)食品安全分析方案核心亮点
2026-03-20
-
【即将实施】2026年3月实施的食品相关标准汇总
2026-02-28
-
【收藏】标准溶液的配制和计算
2026-04-07
-
【必看】灭菌F₀值及其计算方法
2026-03-13
-
独立百天,新生启航:Solstice Advanced Materials中国首秀,锚定先进计算、可持续发展、生命科学新航道
2026年1月末,距离从霍尼韦尔正式分拆独立,并在纳斯达克挂牌上市将满百日时,全新的特种材料公司 Solstice Advanced Materials在上海举办了其独立运营后的首次中国媒体见面会。
作者:张明
-
安捷伦在中国:加速本土创新与绿色发展的双重推进
-
洞察未来,共谋发展 “ 数·智·未来 ” 安捷伦未来实验室媒体圆桌会成功举办
-
食品检验理化常用国家标准与要点
-
水分测定方法开发研究&检测相关问题故障分析解决解读
-
药物常用的晶型表征方法









评论
加载更多