差分脉冲阳极溶出伏安法测定水溶液中Zn2+、Pb2+、 Cd2+含量
重金属元素铅和镉在水体中普遍存在且可长期蓄积危害人体健康。随着人类活动的加剧,环境污染严重,重金属污染事故频发。2005年广东北江流域的镉污染事故、2008年湖南湘江的镉污染事故、2009年陕西凤翔的血铅事件,以及2012年龙江的镉污染事故,都表明了加强对重金属的监测和预警已成为我国环境监测的重点。铅和镉在线检测分析方法目前主要有分光光度法和电化学阳极溶出法。分光光度法易实现自动化,适合应用于在线分析仪,但其灵敏度不足,无法满足铅和镉的痕量分析;电化学溶出伏安法灵敏度高、设备结构简单,被广泛应用于重金属的在线检测中。
金属离子镉(Cd2+)和铅(Pb2+)作为重金属污染源可以对生物机制产生毒性作用从而对人类身体健康造成了严重的威胁。其中Pb 的毒性主要来源于其模仿功能,它可以占据细胞中Ca 依赖蛋白中Ca的结合位点(如钙调节蛋白和蛋白激酶C),导致相应的生理功能不可修复。接触少量的Cd2+,可以导致肾功能失调、骨质疏松、肺气虚、肝损伤和高血压等急性或慢性疾病。因此探索灵敏、快速和简单的分析方法对于精确监控Cd2+和 Pb2+的含量具有重要意义。
检测方法研究进展
目前通常使用的重金属检测方法一般有化学检测法和仪器分析检测法。化学检测法通常是将待测样品与某种化学试剂直接发生化学反应,通过生成物的颜色,生成物在溶液中的聚集状态来判断。随着科学仪器和计算机技术的快速发展,仪器分析在现代分析测试中越来越显出其强大的作用。仪器分析就是采用比较复杂或特殊的仪器设备,通过测量物质的某些物理或物理化学性质的参数及其变化来确定物质的化学组成、成分含量及化学结构,并且各自形成比较独立的方法原理及理论基础的一类分析方法。通常认可的重金属分析方法还有:微谱分(MS)、原子荧光法(AFS)、电感耦合等离子体(ICP)、X荧光光谱法(XRF)、电感耦合等离子质谱法(ICP—MS)法等。不过,这些分析方法都要求借助比较贵重的仪器。样品前期准备工作比较繁琐,现场检测难度较大等。而近年来发展较快的电化学方法在重金属离予检测方面由于其灵敏度高、仪器比较简单、操作方便,是一种很好的痕量分析手段而受到人们越来越多的青睐。本文就重点来介绍这种分析方法。
金属检测的电化学方法
电化学法是近年来发展较快的一种方法,它以经典极谱法为依托,在此基础上又衍生出示波极谱、阳极溶出伏安法等。由于电化学法的检测限较低,测试灵敏度较高,值得推广应用。
极谱分析法是捷克物理化学家海洛夫斯基1922年首先提出的一种电化学分析方法,由于其在发明和发展极谱分析过程的突出贡献而荣获1959年诺贝尔化学奖。自1925年海洛夫斯基制造出全世界第一台极谱仪以来,经过几十年的发展,极谱仪器和分析方法都有了长足的进展。阳极溶出伏安法是一种灵敏度很高、用于痕量组分的电化学分析法。溶出伏安法包含电解富集和电解溶出两个过程。电解富集过程是将工作电极固定在产生极限电流电位上进行电解,使被测物质富集在电极上。为了提高富集效果,可同时使电极旋转或搅拌溶液以加快被测物质快速达到电极表面。富集物质的量取决于电极电位、电极面积、电解时间和搅拌速度等因素。溶出过程是在富集结束静止一段时间后,再在工作电极上施加一个反向电压进行电位扫描,使原来富集在电极上的物质重新氧化为离子进入溶液,在氧化过程中将产生氧化电流,记录下电压—电流曲线(即伏安曲线)。该曲线呈峰形,其峰值电流与溶液中被测离子的浓度成正比,这正是溶出伏安法进行定量分析的依据,而峰值电位可作为定性分析的有力证据。
实验部分
实验原理
溶出分析法可分为阴极溶出分析法、阳极溶出分析法、电位溶出分析法和吸附溶出分析法。本实验采用的是阳极溶出伏安法。
阳极溶出伏安法的测定包含两个基本过程。即首先将工作电极控制在某一条件下,使被测定物质在电极上富集,然后施加线性变化电压于工作电极上,使被测物质溶出,同时记录电流与电极电位的关系曲线,根据溶出峰电流的大小来确定被测定物质的含量。样品离子浓度的计算,是通过计算电流逢高或者面积并且与相同条件下的标准溶液相比较得出。
实验仪器及试剂
仪器:分析天平-FA2004,上海精密科学仪器有限公司;超声波清洗仪-JAC-1505P,上海精密科学仪器有限公司;电化学工作站-CHI832A,上海辰华仪器有限公司;玻碳电极-CHI104,上海辰华仪器有限公司;铂丝电极-CHI115,上海辰华仪器有限公司;Ag-AgCl电极-CHI,上海辰华仪器有限公司。
试剂:氯化镉(分析纯),上海试剂厂;硝酸铅(分析纯),上海试剂厂;氯化锌(分析纯),上海试剂厂;乙酸(分析纯),上海试剂厂;无水乙酸钠(分析纯),上海试剂厂。
电化学工作站参数,见表1
实验过程
1.玻碳电极预处理
用去离子水将玻碳电极在鹿皮上抛光表面3 min,再使用Al2O3粉乳浊液抛光表面3 min,然后用蒸馏水超声清洗1 min,晾干待用。
2.标准溶液配制
镉标准溶液:称取 0.4575 g 氯化镉,放入烧杯中,加入去离子水溶解,冷却移入 250 mL 容量瓶,定容,摇匀,倒入试剂瓶中备用。此溶液浓度为1x10-2mol/L。
铅标准溶液:秤取0.8281 g硝酸铅,放入烧杯中,加入去离子水溶解,冷却转移入250 mL容量瓶中,定容,摇匀,倒入试剂瓶中备用。此溶液浓度为1×10-2mol/L。
锌标准溶液:秤取0.3408 g氯化锌,放入烧杯中不,加入去离子水溶解,冷却转移入250 mL容量瓶中,定容,摇匀,倒入试剂瓶中备用。此溶液浓度为1×10-2mol/L。
缓冲溶液:称取无水乙酸钠32.5 g加水稀释,使用乙酸溶液调节溶液PH为4.8,冷却,后移入250 mL容量瓶,定容,摇匀,最后倒入试剂瓶中备用。
3.单一离子的测定
■ 镉标准曲线的绘制
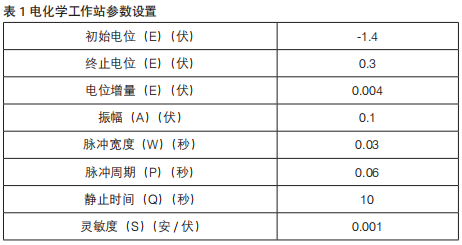
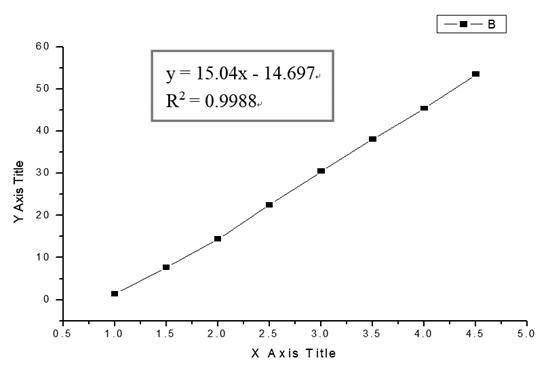
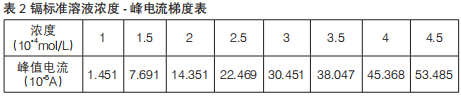
吸取20 mL标准缓冲溶液于三电极系统中,依次加入0.1 mL镉标准溶液测定峰值电流,重复操作8次,详见图1。以峰值电流为纵坐标,溶液中的镉含量为横坐标绘制标准曲线,详见图2和表2。
图1 镉标准溶液溶出伏安图
图2 镉标准曲线图
■ 铅标准曲线的绘制
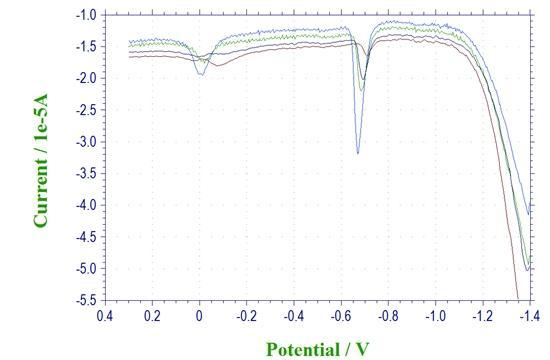
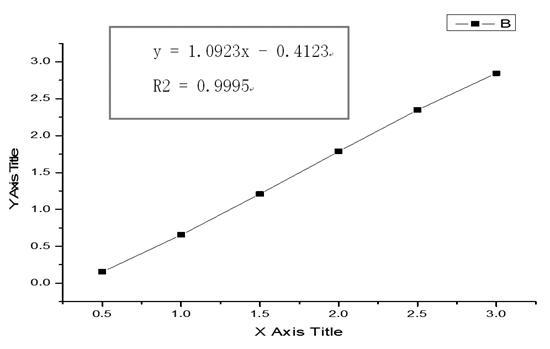
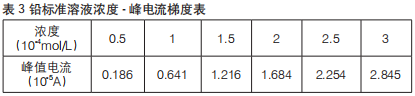
吸取20 mL标准缓冲溶液于三电极系统中,依次加入0.1mL铅标准溶液测定峰值电流,重复操作6次,详见图3。以峰值电流为纵坐标,溶液中的铅含量为横坐标绘制标准曲线,详见图4和表3。
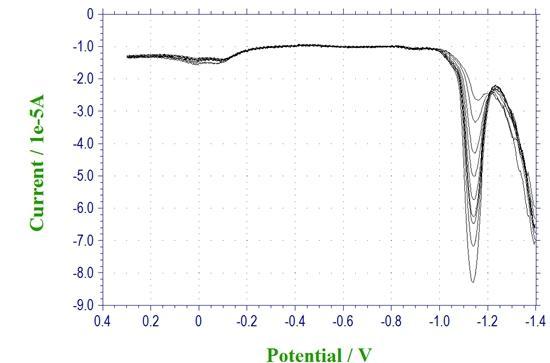
图3 铅标准溶液溶出伏安图
图4 铅标准曲线图
■ 锌标准曲线的绘制
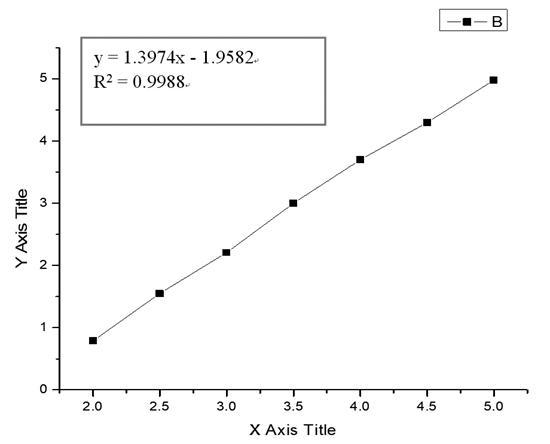
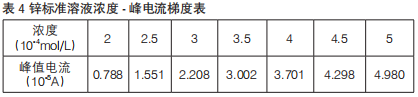
吸取20 mL标准缓冲溶液于三电极系统中,依次加入0.1 mL锌标准溶液测定峰值电流,重复操作7次,详见图5。以峰值电流为纵坐标,溶液中的锌含量为横坐标绘制标准曲线,图6和表4。
图5 锌标准溶液溶出伏安图
图6 锌标准曲线图
4.三种离子共存时测定
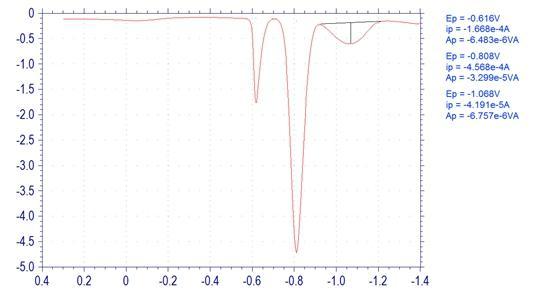
在最优实验条件下,配置未知浓度的Pb2+、Cd2+和Zn2+溶液,同样按照实验方法进行测定,三种离子的溶出伏安曲线如图7所示。
图7 三种离子共存溶出伏安图
计算结果:
C(Pb2+)=15.6297x10-4mol/L
C(Cd2+)=4.0144x10-4mol/L
C(Zn2+)=4.4017x10-4mol/L
实验讨论
差分脉冲溶出伏安法在富集过程中,各个离子按照还原性强弱的顺序依次在电极表面还原,所以离子的浓度和还原性强弱决定了还原在电极表面的浓度,还原越多的离子再氧化溶出时溶出峰电流值越大,但是溶液中的共存离子在电极表面的竞争吸附会影响待测离子的沉积,进而影响溶出伏安响应。所以在实际检测中多种离子共存时,应考虑离子之间的相互影响,采用混标水样绘制的相应工作曲线,这样测定结果才更科学可靠。
实验与分析
展源
何发
相关文章
-

AAS法分析茶叶中的铅,镉,砷
2020-05-27
-
石墨炉法测定油脂中的重金属元素
2020-05-27
-

ICP-MS 法法测定水质中的重金属元素
2020-05-27
-

重金属污染的快速分析
2020-05-27
-

重金属污染的快速分析
2020-05-27
-

痕量有害重金属元素的检测
2020-05-27
-

高效测定油脂中的重金属元素
2020-05-27
-

【新老方法PK】土壤重金属污染检测技术汇总
2021-03-23
-

土壤中有害重金属分析方法
2020-05-27
-
水质中的重金属元素的测定
2020-05-27

加载更多