多肽药物|1|:什么是多肽药物?
▉ 什么是多肽药物
Peptide(多肽)源于希腊语"peptós/digested",是指通过酰胺键或肽键相连的氨基酸(AAs)链。共价肽键是氨基酸通过缩合反应形成的,一个氨基酸的a-羧基基团与另一个氨基酸的a-氨基基团缩合产生水形成肽键。肽链中的一个氨基酸单位称为“残基”。肽键的形成导致水的流失。肽的“主干”是肽键,侧链是可变的,它也是蛋白质水解的中间产物。
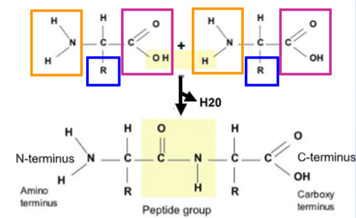
蛋白质包含多个肽链, “多肽”和“蛋白质”有时可以相互替换使用。一般分子量(MWs)小于10,000道尔顿或少于50个AA的分子称为多肽,超过该数值则称为蛋白质,介于小分子化学药和蛋白类药物之间。
▉ 肽类药物发展史
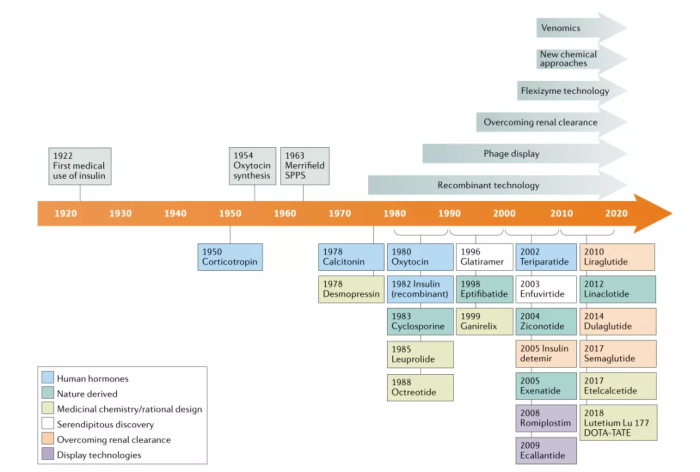
1922年,第一个肽类药物是从牛和猪的胰腺中提取的胰岛素,用于1型糖尿病的治疗。1954年,Vincent du Vigneaud的团队发表了《the total synthesis of oxytocin and vasopressin》(1955年获得诺贝尔化学奖),多肽首次被化学合成。
另一个飞跃是Bruce Merrifield通过在固相上组装氨基酸来自动合成肽,这导致了1963年固相肽合成(SPPS)的发明(1984年获得诺贝尔化学奖)。20世纪80年代重组技术的出现使生产更大的多肽成为可能。
随后,通过结合脂类、较大的蛋白质和聚乙二醇来增加多肽分子量的策略有助于克服肾脏清除和增加血浆循环时间的问题。像噬菌体展示这样的显示技术现在允许从巨大的文库中以目标为导向发现具有更多药物性质的多肽。Flexizyme技术允许将非蛋白原性氨基酸纳入展示库。
天然肽的发现,特别是蛇毒肽的发现,以及新的化学方法也在推动这一领域的发展。
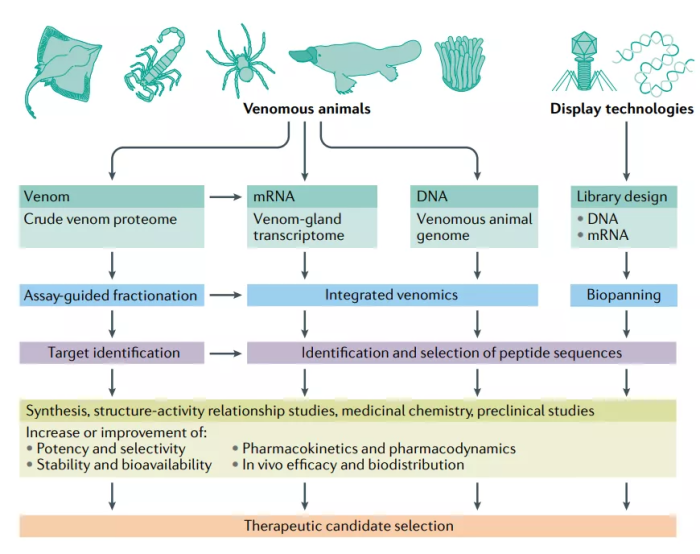
▉ 肽类药物发现策略
整合的毒液组学和显示技术是发现治疗性先导物的两项关键技术。
整合毒液组学利用生物信息学分析有毒动物的基因组和转录组数据,以及从粗毒液样本中获得的蛋白质组学数据。该方法可以识别大量的毒液肽序列,然后合成或重组生成,并可用于治疗靶标的筛选。
显示技术可以产生大量针对治疗靶点的肽库。这一过程通常经过几轮筛选后产生高亲和力的靶结合物。然后使用药物化学策略来改善这些先导物的药物性质。

常见的多肽药物
从生理生化角度来看,多肽是涉及生物体内各种细胞功能的生物活性物质,是生命活动不可或缺的参与者,目前已有超过7,000 种天然多肽被发现,涉及到激素、神经、细胞生长和生殖等各个领域。
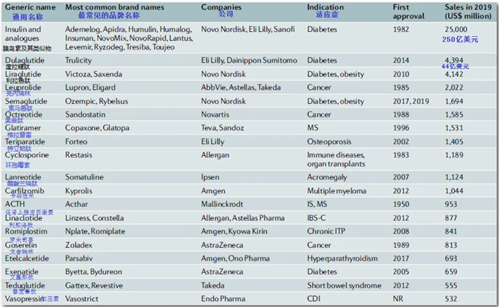
多肽药物的主要治疗领域及品种具体情况如下:
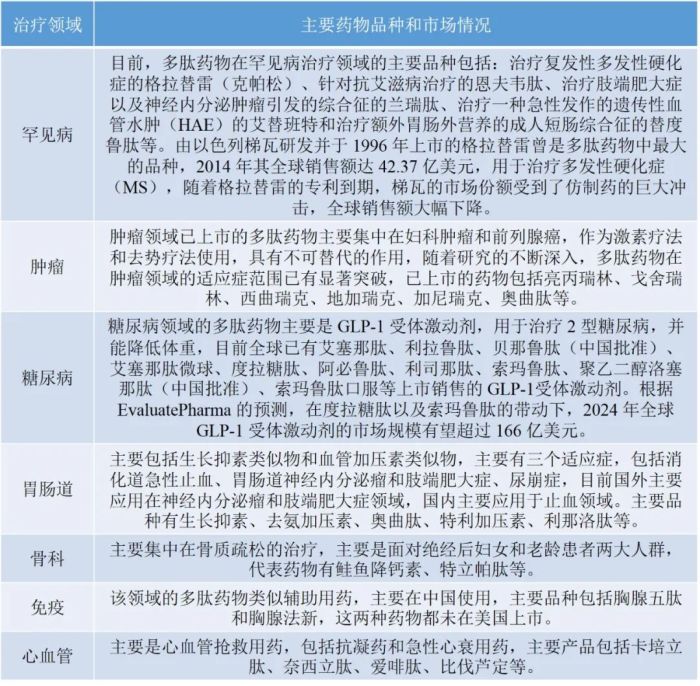
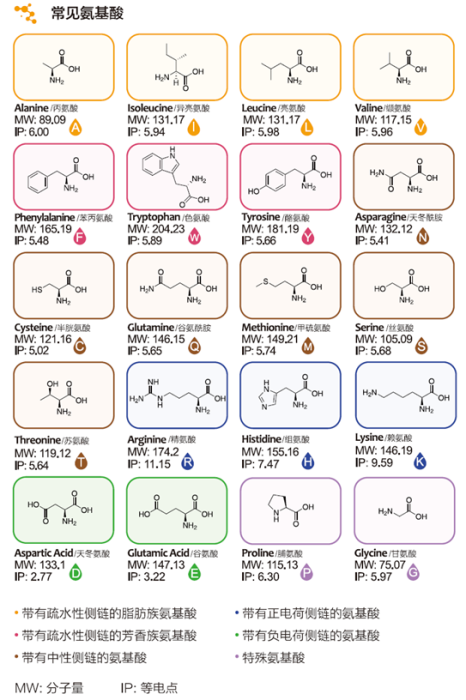
▉ 多肽中常见的氨基酸
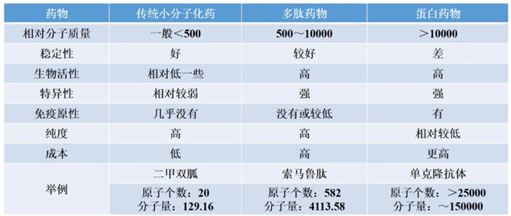
▉多肽药物与其它药物的对比
多肽药物主要来源于内源性多肽或其他天然多肽,结构清晰、作用机制明确,相对于一般的小分子化药,具有更高的活性和更强的选择性,在治疗复杂疾病方面优势明显,且由于多肽本身是氨基酸组成的化合物,其代谢产物为氨基酸,对人体一般没有副作用或副作用很小。
相对于蛋白质药物,多肽药物具有稳定性相对较好、纯度高、生产成本低、免疫原性较低或无免疫原性等优势,质量控制水平也能接近于传统的小分子化药。
END
质谱学堂
展源
何发
相关文章
-

多肽药物技术发展与市场分析
2023-02-17
-

多肽类药物的药代动力学研究
2020-05-27
-

蛋白多肽类药物的药代动力学研究
2020-05-27
-

QC, IQC, IPQC, QA,到底是什么鬼?
2020-05-27
-

AAS法分析茶叶中的铅,镉,砷
2020-05-27
-

关于多肽纯化的问题解答
2021-01-11
-
(3).jpg?x-oss-process=image/resize,m_pad,w_80,h_60,color_eeeeee)
多肽纯化十问十答
2020-05-27
-

聚乙二醇化提高多肽的药效
2020-05-27
-

聚乙二醇耦合提高多肽的药效
2020-05-27

加载更多